-
Alta luz
461432-26-8 intermedios farmacéuticos
,Intermedios farmacéuticos C21H25ClO6
,Intermedios farmacéuticos de Dapagliflozin
-
Nombre de productoDapagliflozin
-
SinónimosDAPAGLIFLOZIN; (1S) - [4-chloro-3- [(4-ethoxyphenyl) metilo] fenilo 1,5-Anhydro-1-C-] - D-glucitol;
-
CAS461432-26-8
-
Frecuencia intermediaC21H25ClO6
-
MW408,88
-
EINECS639-683-0
-
Punto de ebullición°C 609.0±55.0 (previsto)
-
Densidad1,349
-
Purezael 99%
-
Lugar de origenChina
-
Nombre de la marcaRUN
-
CertificaciónIOS9001
-
Número de modeloRUN-Z
-
Cantidad de orden mínima10g
-
Precioinquiry
-
Detalles de empaquetado10g 50g 100g 500g 1kg
-
Tiempo de entrega3-7 días
-
Condiciones de pagoT/T, MoneyGram, BTCcoin
-
Capacidad de la fuente1kg --100kg
461432-26-8 Dapagliflozin S1548 Selleck C21H25ClO6 639-683-0
SECCIÓN 1: Información básica
| Información básica de Dapagliflozin |
| Interacciones medicamentosas farmacológicas de la seguridad del método de la síntesis de la farmacinética de los efectos de las drogas de la diabetes |
| Nombre de producto: | Dapagliflozin |
| Sinónimos: | DAPAGLIFLOZIN; (1S) - [4-chloro-3- [(4-ethoxyphenyl) metilo] fenilo 1,5-Anhydro-1-C-] - D-glucitol; Propanediol de Dapagliflozin; BMS-512148-05; Dapagliflozin S1548 Selleck; BASE DE DAPAGLIFLOZIN; Daglican; Dapagliflozi |
| CAS: | 461432-26-8 |
| Frecuencia intermedia: | C21H25ClO6 |
| MW: | 408,88 |
| EINECS: | 639-683-0 |
| Categorías de producto: | Inhibidores; Otros APIs; APIs; Compuestos aromáticos; Heterocycles; Intermedios y sustancias químicas finas; Productos farmacéuticos |
| Mol File: | 461432-26-8.mol |
| Propiedades químicas de Dapagliflozin |
| Punto de ebullición | °C 609.0±55.0 (previsto) |
| densidad | 1,349 |
| pka | 13.23±0.70 (previsto) |
| Información de seguridad |
| Uso y síntesis de Dapagliflozin |
| Drogas de la diabetes | Dapagliflozin (ForxigaTM) es una nueva droga antidiabética desarrollada en común por Bristol-Myers Squibb y AstraZeneca, siendo aprobado por la agencia de medicinas europeas (AME) el 12 de noviembre de 2012. Es también el primer inhibidor aprobado SGLT2 para el tratamiento del diabetes tipo II, siendo una opción importante en el tratamiento de la diabetes, y se utiliza para mejorar control glycemic como adjunto a dietético y el ejercicio para los adultos con diabetes tipo II. Dapagliflozin es un inhibidor del co-transportador 2 de la sodio-glucosa. El 8 de enero de 2014, los E.E.U.U. Food and Drug Administration (FDA) lo han aprobado para ser utilizada en el tratamiento del diabetes tipo II. Mientras tanto, el FDA requiere a los productores conducir la investigación posterior a la comercialización sobre riesgos relacionados con drogas. El ensayo posterior a la comercialización pedido por el FDA incluye un ensayo cardiovascular del resultado para evaluar el riesgo cardiovascular para los pacientes de alto riesgo después del tratamiento con el dapagliflozin en la línea de fondo y un estudio para evaluar el riesgo de cáncer de vejiga en pacientes reclutados. Otro estudio evaluará el efecto tumor-que promueve de la vejiga de esta droga sobre animales del roedor. Dos estudios evaluarán la farmacinética, la eficacia y la seguridad del dapagliflozin en pacientes pediátricos; un sistema del programa fortalecido de la farmacovigilancia supervisará anormalidades del hígado e informes del resultado del embarazo en los pacientes que reciben daglitazone. Dapagliflozin será comercializado debajo de la marca registrada Farxiga por la farmacia de Haoeyou. La información antedicha es corregida por Andy del chemicalbook. |
| Efectos farmacológicos | Dapagliflozin trabaja a través del transportador de inhibición 2 (SGLT2), una proteína de la sodio-glucosa en el riñón que reabsorba la glucosa en la circulación sanguínea. Esto permite que la glucosa adicional sea excretada a través de la orina, mejorando control glycemic sin la secreción cada vez mayor de la insulina. El uso de esta droga requiere a pacientes con la función renal normal mientras que los pacientes de moderado a la escasez renal severa deben ser discapacitados utilizar esta droga. El solo uso de este producto o combinación con metformin, pioglitazone, glimepiride, la insulina y otras drogas puede reducir perceptiblemente el HbA1c y la glucosa en sangre de ayuno de los pacientes que sufren diabetes tipo II. La frecuencia de la reacción adversa era similar al placebo con poco arriesgado de la hipoglucemia, pudiendo reducir el peso corporal. La eficacia del dapagliflozin es comparable con los inhibidores de la peptidasa del dipeptidyl, y varias nuevas drogas hipoglicémicas, y puede también bajar suavemente la presión arterial y el peso corporal. La droga tiene 5mg y las tabletas 10mg dos a elegir de, se pueden utilizar solamente o así como la insulina, incluyendo otras drogas de la diabetes. |
| Farmacinética | En temas sanos, el dapagliflozin fue absorbido rápidamente después de la administración oral con un rato máximo Tmax que era 1 a 2 horas, un índice del atascamiento de la proteína del 91%, una biodisponibilidad oral del cerca de 78% y una semivida terminal del plasma de 12,9 horas. Después de la administración oral, la droga es metabolizada principalmente por el glucuronosyltransferase 1A9 (UGT1A9) del difosfato de la uridina en el metabilito inactivo en el hígado con la parte más pequeña que es metabolizada por la enzima P450 y de ningún efecto inhibitorio o de inducción sobre la enzima P450. Los prototipos de la droga y los metabilitos relacionados fueron excretados a través de la orina (el 75%) y de las heces (el 21%). Compare la administración simultánea de este producto con la comida de alto grado en grasas y con la administración de ayuno, Tmax se puede ampliar por 1 doblez, pero la absorción no afectó al grado, así que se puede administrar así como la comida. La farmacinética del daglitazone fue afectada perceptiblemente por la función renal. Combinan a los pacientes diabéticos con la escasez renal suave, moderada o severa para estar conforme a la administración oral del magnesio 20 • daglitazone d-1 por 7 días. La cantidad sistémica mala de la exposición, comparada con los pacientes con la función renal normal, es respectivamente el 32%, el 60% y el 87% más altos. Para los pacientes con la función renal normal, la escasez suave, la escasez moderada y la escasez severa, la cantidad urinaria de la excreción de la glucosa en 24 horas de estado estacionario era 85, 52, 18 y 11g, sucesivamente. Kasichayanula y otros han estudiado los efectos farmacocinéticos de la disfunción del hígado sobre daglitazone. Los pacientes con la escasez hepática suave, moderada y severa que tenía una sola dosis oral del magnesio 10 del daglitazone, el Cmax de cada grupo eran los 12% bajan, los 12% más altos y los 40% más altos que ése con la función hepática normal, respectivamente. El AUC de cada grupo era perceptiblemente más alto que el de la función hepática normal por el 3%, el 36% y el 67%. Por lo tanto, no se recomienda para aplicar daglitazone a los pacientes de la disfunción renal moderada y severa. Los pacientes severos de la disfunción del hígado necesitan reducir el uso de la dosis. |
| Método de la síntesis | el ácido 5-bromo-2-chlorobenzoic está conforme a la desinfección con cloro acylating, y tiene reacción de los Friedel-artes con el éter feniletil para la reducción de su grupo de carbonyl, generando el metano de 5 bromo-2-chloro-4'-ethoxydiphenyl, sujetando más lejos a la condensación con 2, 3, 4, 6 acid-1,5-lactone tetra-O-trimetilsililes-D-GLUCOPYRANOSANOIc. El grupo de hidróxido anomérico del carbono está conforme a la eterificación y al deprotection para dar 2 chloro-5- (1-methoxy-D-glucopyranose-I-yl) - 4' - ethoxydiphenylmethane, y entonces utilizar Et3SiH/BF3 • OEt2 para que reducción quite methoxy, seguido por la esterificación y la hidrólisis acéticas del anhídrido para dar a agentes hipoglicémicos daglitazone con la producción total del cerca de 40%.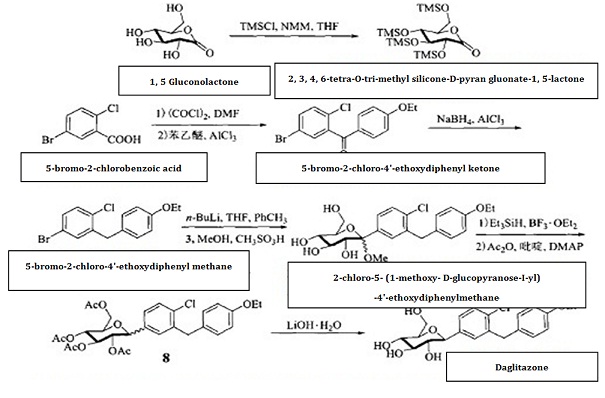 Fig.1 muestra la ruta de la reacción química de sintetizar el dapagliflozin. |
| Seguridad | Daglitazone tiene tolerancia y seguridad excelentes con la incidencia de los acontecimientos adversos asociados al magnesio 10 • daglitazone d-1 que es similar al del placebo. Los acontecimientos adversos comunes incluyeron hipoglucemia, polyuria, dolor de espalda, aumento genital de las infecciones, de las infecciones de vías urinarias, del dyslipidemia y del hematócrito (HCT). El riesgo total de hipoglucemia es bajo, y la incidencia de la hipoglucemia se asocia a otros agentes hipoglicémicos básicos. La incidencia de la hipoglucemia era más alta en los pacientes que sujetaban para articular el tratamiento entre el daglitazone y los sulfonylureas o insulina comparados con placebo. Por lo tanto, cuando este producto se utiliza conjuntamente con la insulina o el secretagogue de la insulina, usted puede necesitar ajustar la dosis de la última. |
| Interacciones medicamentosas | Este producto es metabolizado principalmente en el hígado por el metabolismo UGT1A9, siendo el substrato de la P-glicoproteína. El estudio confirmó que la farmacinética del daglitazone no fue afectada por metformin, pioglitazone, sitagliptin, glimepiride, voglibose, y simvastatin, valsartan, warfarin, y digoxin. Las concentraciones del suero de las drogas antedichas no son también clínico perceptiblemente afectadas por daglitazone. Rifampicin puede reducir la cantidad de la exposición de daglitazone por el 22% mientras que el ácido mefenámico puede aumentar la cantidad de la exposición del cuerpo en el 51%, pero tiene no clínico efecto significativo sobre 24 excreciones de la glucosa de la orina de h. |
| Descripción | La administración terapéutica australiana de las mercancías (TGA) y la Comisión Europea aprobaron el dapagliflozin en octubre y noviembre de 2012, respectivamente, como adjunto para adietar y para ejercitar para el tratamiento del tipo - diabetes 2. Dapagliflozin es una terapia potencialmente atractiva debido a su mecanismo glucosesensitive y de la insulina-independiente de la acción. Es un inhibidor selectivo SGLT2 de la primero-en-clase (IC50=1.1nanómetro; selectividadcontraSGLT1>1000)quebajaelumbralrenalparalareabsorciónde laglucosa, permitiendo queexcesode laglucosasea eliminadavíalosriñones. Enratasnormales, laadministracióndeldapagliflozinpromuevelaexcrecióndosis-dependientedelmagnesiohasta1900de laglucosadurante24períodosdeh, conefectoamaximalen3mg/kg. Enunratmodelde ladiabetes, tratamiento previoconlosresultadospancreáticosdelstreptozotocinde latoxinaenlahiperglucemiaquees reducidael55%porlaadministraciónde unasoladosisde0,1mg/kgdeldapagliflozincomparadaconelvehículo. Losinhibidoresarilesdel O-glucósidoSGLT2eranprincipiantestempranosenlaclínica, peroelacoplamientoarildel C-glucósidoencontradoendapagliflozinconfiereresistenciaalmetabolismoglucosidasa-mediadoque llevaa lautilidadclínicamejoradaen relación conlos O-glucósidosariles. Elacoplamientomodificadode la carbohidrato-agluconarequirióelajusteconcomitantede unortoa unarylglucosidemeta-substituidoalcanzarlainhibiciónpotenteSGLT2. Dapagliflozinfue sintetizadoenvariospasosvíalareacciónde unaryllithiumcongluconolactonapor-silylatedpara formarelacoplamientodominantedel C-glucósido. Unareducciónalfa-selectivadelglucósidoanoméricoresultantedioelbeta-Carylglucosidedeseada. Elmetabilito(inactivo)decirculaciónprincipaleselresultadode3-O-glucuronidationdelglucosylmoiety. De losmetabilitosde laminoría, delresultadooxidativoprincipalde laespeciedeO-dealkylationdel ethoxy-grupoyde lahidroxilaciónde lamitaddelbiarylmethane. |
| Propiedades químicas | Sólido blanco |
| Autor | Bristol-Myers Squibb (Estados Unidos) |
| Aplicaciones | Un inhibidor del transportador 2 de la sodio-glucosa. |
| Aplicaciones | terapéutico para la diabetes yo o II, y la hiperglucemia |
| Definición | ChEBI: A.C. - beta-D-glucosa que comprende glycosyl en la cual a un grupo de fenilo de 4 chloro-3- (4-ethoxybenzyl) substituye al grupo hidroxi anomérico. Utilizado (en el formo f su monohidrato del propanediol) para mejorar ontrol glycemic, junto con dieta y ejercicio, en adultos con el tipo - diabetes 2. |
| Marca | Forxiga |